10.รูปร่างพันธะ
โมเลกุลโคเวเลนต์ มีรูปร่างแตกต่างกัน ข้นอยู่กันแรงผลักภายในโมเลกุึลของอิเล็กตรอนชคู่ร่วมพันธะและอิเล็กตรอนคู่
โดดเดี่ยวรอบอะตอมกลาง
หลักในการชคิดรูปร่างพันธะ
1.ถ้านับจำนวนพันธะได้ 2 จะเป็นรูปเส้นตรงหรือมุึมงอ โดดจะเป็นเส้นตรงก็ต่อเมื่อไม่มีอิเล็กตรอนคู่โดดเดี่ยวที่อะตอม
กลาง แต่ถ้ามีอิเล็กตรอนคู่โดดเดี่ยวขจะเป็นรูปมุึมงอ ดังเช่น
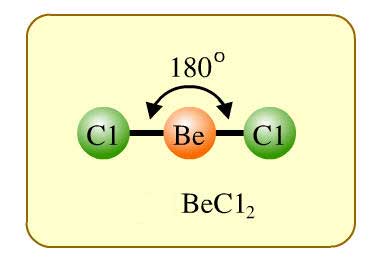 หรือ
หรือ 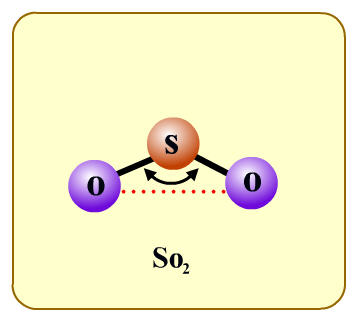
2.ถ้านับขจำนวนได้ 3 พันธะจะเป็นรููป 3 เหลี่ยมแบนราบหรือพีรมิดฐานสามเหลี่ยม โดดจะเป็นสามเหลี่ยมแบนราบก็ต่อ
เมื่อไม่มีอิล็กตรอนคู่โดดเดี่ยวที่อะตอมกลาง แต่ถ้ามีอิเล็กตรอนคู่โดดเดี่ยว 1 คู่ จะเป็นรูปพีรมิดฐานสามเหลี่ยม ดังเช่น
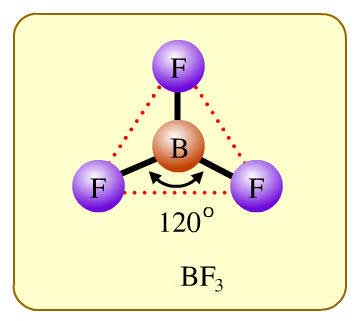 หรือ
หรือ 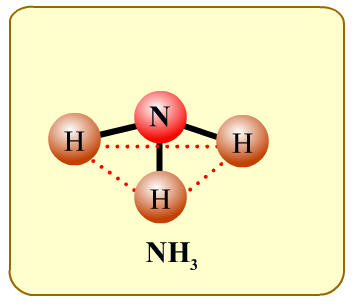
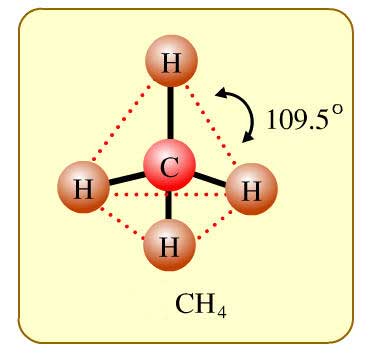
3.ถ้านับจำนวนพันธะได้ 4,5,6 จะเป็นรุปทรง 4 หน้า พีรมิดคู่ฐนาสามเหลี่ยม และทรง 8 หน้า ตามลำดับ(ในกรณีที่อะตอม
กลางไม่มีคู่โดดเดี่ยว) ดังเช่น
ทรง 4 หน้า
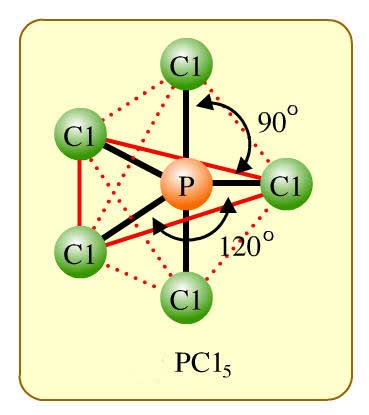
พีรมิดคู่ฐานสามเหลี่ยม
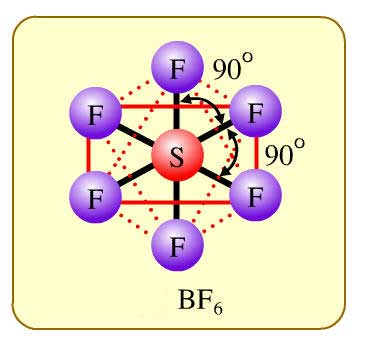
ทรง 8 หน้า
4.ถ้าสารประกอบใดอะตอมกลางเกิด 1 ตัวขึ้นไปให้เอาอะตอมกลางที่มีจำนวนพันธะมากที่สุึด เป็นหลักในการพิจารณารูป
ร่างพันธะ
